Tricine-SDS-PAGE制胶及电泳试剂盒
储存条件:参照产品组成储存条件,保质期1年。
产品内容:
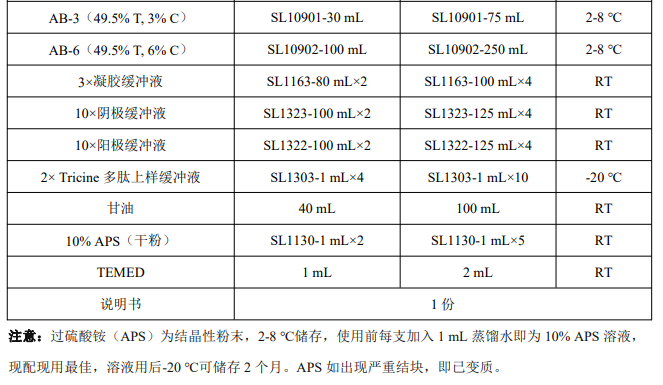
产品说明:
Tricine-SDS-聚丙烯酰胺制胶及电泳试剂盒(Tricine-SDS-PAGE)是目前电泳法变性分离多肽的主要方法,适用于低分子量蛋白(2.5-40 kD)蛋白的分离。此试剂盒可以制备 20 或 50 块 0.75 mm× 14 cm×14 cm胶。对于大于 5 kD 的蛋白,无需制备隔离胶,双层胶足以分离。对于小于 5 kDa 的蛋白,需要制备 3 层胶才能较好的分离。推荐使用 4%浓缩胶,10%隔离胶,16%分离胶作为标准浓度,可以分辨出 1-5 kD 的片段。Tricine-SDS-PAGE 系统不同于常规的 SDS-PAGE,使用两种缓冲液电泳,电泳槽内槽是 1×阴极缓冲液,含有 Tricine 和 SDS。外槽是 1×阳极缓冲液,为 0.2M Tris。
操作步骤:(以足够灌两块 0.75 mm× 14 cm×14 cm 胶为例)
一、制胶
标记 3 个 50 mL 三角瓶,按下表用量配制分离胶 30 mL、隔离胶 9 mL 和浓缩胶 9 mL。混匀后真空脱气 10-15 分钟。
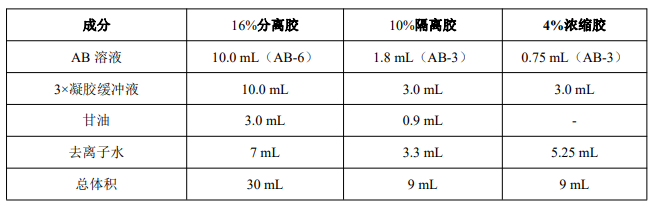
2. 在分离胶瓶中加入 10% APS 150 μL 溶液和 TEMED 30 μL,轻旋混匀。
3. 灌分离胶。用巴斯德吸管,将分离胶溶液沿着隔条边缘缓缓注入,直至距玻璃上沿约 5 cm。由于分离胶比重比隔离胶大,故可在其凝固前直接灌隔离胶。
4. 在隔离胶瓶中加入 10%的 APS 溶液 75 μL 和 TEMED 15 μL,轻轻旋转混匀。
5. 灌隔离胶。用巴斯德吸管,将隔离胶溶液沿着隔条边缘缓缓注入,直至距玻璃板上沿约 3 cm。
6. 加入 1 cm 高的水饱和异丁醇封胶。室温放置 30-45 分钟。(氧气会抑制胶凝固;水饱和异丁醇可用水代替,但效果会差一些)。
7. 在浓缩胶瓶中加入 10% APS 溶液 75 μL 和 TEMED 15 μL,轻轻旋转混匀。
8. 灌浓缩胶。用巴斯德吸管,将浓缩胶沿着隔条边缘缓缓注入,直至距玻璃板上沿约 1 cm 。
9. 插入 0.75 mm 厚梳子,补加浓缩胶溶液填满梳子间的空隙,通过抽真空或者吸水滤纸去除气泡。静置30-45 分钟确认凝胶后小心拔出梳子。
二、加入电泳缓冲液
1. 在上层缓冲液槽中加入 1× 阴极缓冲液,并用 1× 阴极缓冲液冲洗加样孔注:10× Tricine-SDS-PAGE 阴极缓冲液用去离子水 1:9 稀释成 1×阴极缓冲液。
2. 在下层缓冲液槽中加入 1× 阳极缓冲液。
注:10×Tricine-SDS-PAGE 阳极缓冲液用去离子水 1:9 稀释成 1× 阳极缓冲液。
三、上样
1. 处理样品。如样品是蛋白沉淀物,则加入 50-100 μL 新配的 1×上样缓冲液溶解。如果样品是蛋白稀溶液,则需先浓缩蛋白,再与 2× Tricine 多肽上样液按 1: 1 混合。
2. 100 ℃煮沸 3-5 分钟灭活蛋白酶;膜蛋白则需 37℃孵育 15-60 min。
注意:与上样缓冲液混合后的样品如未经灭活蛋白酶,切勿室温放置。
3. 上样。如需考染,复杂蛋白样品建议上样量 20 μL(含 25-50 μg 总蛋白);含一种或几种蛋白的样品,建议上样量 1-10 μL。如需银染,上样量可相应减少 10-100 倍。
四、电泳
1. 电泳。首先 30 V 恒压电泳 1 h, 然后 150 V 恒压电泳 4-5 h。
注:上样液以考马斯亮蓝 G-250 为指示剂,其迁移速度要快于最小的肽。
2. 终止电泳,取出凝胶进行后续的实验(建议银染染色,节约样品)。
注意:考染或银染时,尽可能采用快速染色方法,否则多肽有可能会扩散出 PAGE 胶而降低检测的灵敏度。
本产品只适用于科研,不能用于临床诊断。严禁用于临床医疗及其他非科研用途!
 在线客服1号
在线客服1号