蛋白质是包括人类在内的各种生物有机体的重要组成成分,是生命的物质基础之一。生物体的生长、发育、遗传和繁殖等一切生命活动都离不开蛋白质。
随着分子生物学、结构生物学、基因组学等研究的不断深入,人们意识到仅仅依靠基因组的序列分析来试图阐明生命活动的现象和本质是远远不够的。只有从蛋白质组学的角度对所有蛋白质的总和进行研究,才能更科学地掌握生命现象和活动规律,更完善地揭示生命的本质。
由此许多学者将生命科学领域的研究焦点从基因转向蛋白质,使蛋白质成为揭示生命活动现象和分子生物学机理的重要研究对象。研究蛋白质首要的步骤是将目的蛋白从复杂的大分子混合物中分离纯化出来,得到高纯度具有生物学活性的目的物。因此,高效的纯化技术和手段是蛋白质研究的重要基础和关键之一。
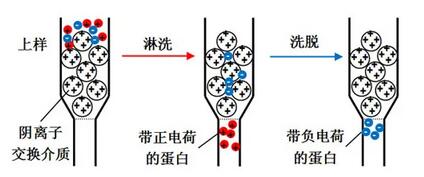
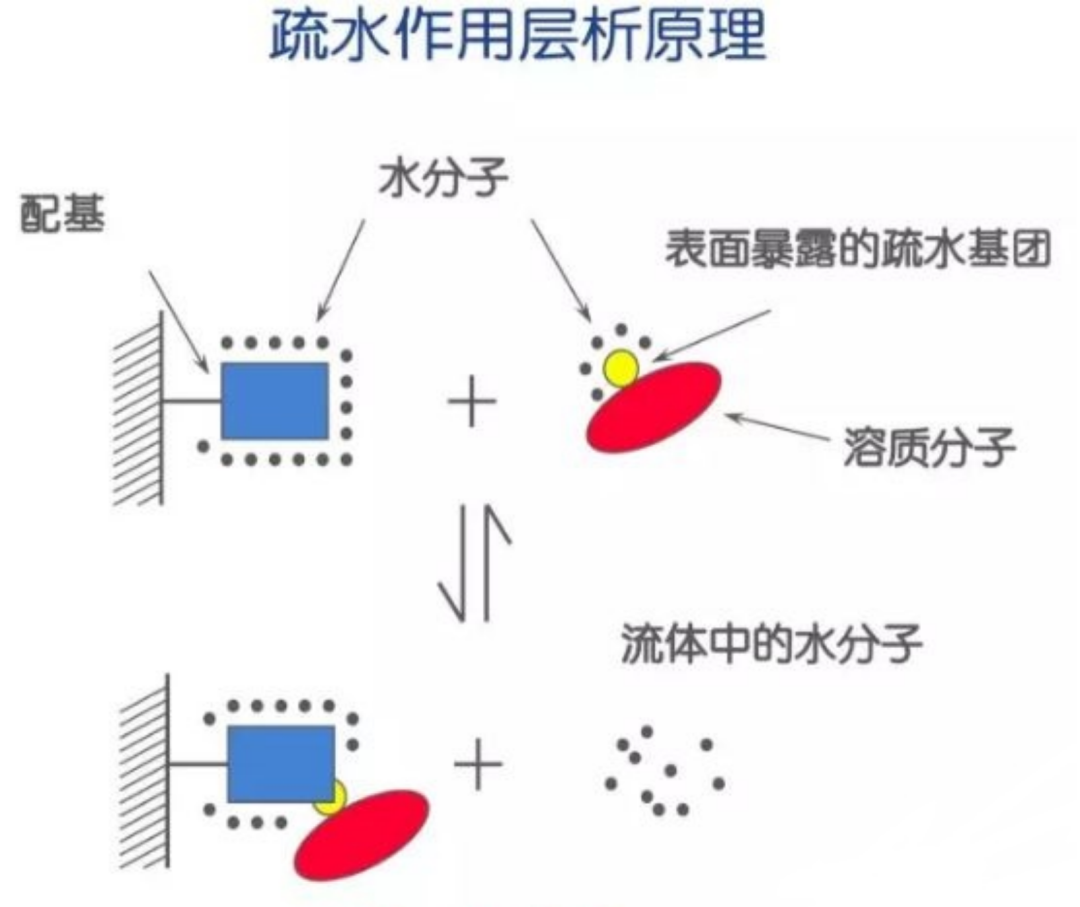
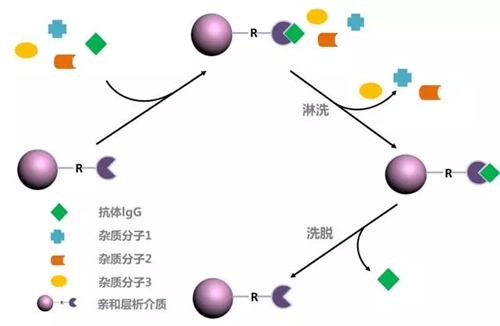
凝胶过滤层析(又叫做分子筛)是根据样品的分子大小对样品进行分离的一种简单温和的层析技术。凝胶过滤层析也称分子筛层析、排阻层析,是利用具有网状结构的凝胶的分子筛作用,根据被分离物质的分子大小不同来进行分离。不同于离子交换层析和亲和层析,凝胶过滤的层析样品不与层析柱料结合,因此,缓冲液成分不直接影响分辨率。 原理:层析柱中的填料是球状颗粒的惰性的多孔网状结构的柱料,多是交联的聚糖(如葡聚糖或琼脂糖)类物质。在加入样品之后,样品中的小分子物质能进入球状填料内部,在柱子中停留时间较长;而大分子物质不能进入球状填料内部,停留时间较短。所以当样品经过凝胶过滤层析柱分离后,样品中的不同分子大小的物质就可以被分离开了。 图1:凝胶过滤层析过程示意图 特点: 根据分子大小和形状进行分离 是一种非吸附的分离方式 缓冲液成分不直接影响分辨率,只需要一种缓冲液 操作便捷 离子交换层析是目前蛋白质分离纯化中应用最广泛的方法之一。 原理:不同蛋白等电点差异,分子大小差异,在同一流动相中电荷密度分布不同,电荷量不等,与具有相反电荷的离子交换介质结合强度不同,在流动相洗脱时保留时间不同,从而得以分离。 图1:离子交换层析过程示意图 特点: 根据分子大小和等电点差异进行分离 灵敏度高,重复性,选择性好,分析速度快 原理:疏水层析是依据蛋白质疏水性差异分离的。即根据蛋白质和疏水介质表面的疏水基团的可逆相互作用进行分离。蛋白的疏水性在高离子强度下被增强,因此在高离子强度环境中结合,通常采用降低离子强度的方式进行洗脱。独特的吸附分离模式使得疏水层析成为硫酸铵盐析后或离子交换高盐洗脱后理想的纯化方式。 图1:疏水层析原理图 特点: 采用了盐的水溶液作为流动相,色谱条件温和,生物大分子的活性回收率很高。 蛋白质在HIC操作过程中是高盐上样,低盐洗脱(高盐浓度的样品不必作处理就可直接上样)。 在一次色谱中可同时实现出去盐酸胍、蛋白质复性和分离三个目的。 温度升高,蛋白质天然折叠伸展,暴露出更多内部疏水集团,使蛋白质的HIC保留发生变化。 色谱填料稳定性好,盐水体系作流动相无环境污染。 原理:亲和层析是应用生物高分子与配基可逆结合的原理,将配基通过共价键牢固结合于载体上而制得的层析系统。这种可逆结合的作用主要是靠生物高分子对它的配基的空间结构的识别。常用的生物亲和关系有酶-底物、底物类似物、抑制剂、激活剂、辅因子,抗体-抗原,激素-受体蛋白、载体蛋白,外源凝集素-多糖、糖蛋白、细胞表面受体,核酸-互补核苷酸序列、组蛋白、核酸结合蛋白等,具有高效、简单、快速的优点,是当前最为理想的分离纯化蛋白的方法。 图1:亲和层析原理图 以上四种蛋白纯化的方法,在这里就简单给大家介绍一下,详细的实验操作步骤及注意事项,后期会给大家介绍,请持续关注我的动态哦!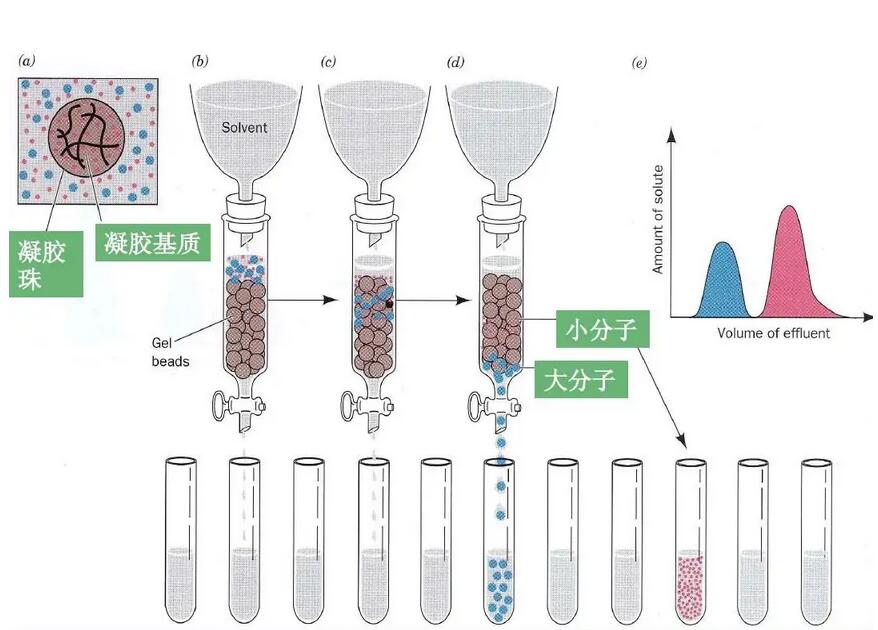
 在线客服1号
在线客服1号



